Kyoto Sangyo University
京都産業大学 生命科学部
先端生命科学科 研究者クローズアップ
「”くすり”で解き明かす、消化管と膀胱の精密なメカニズム」
— なぜ腸は「第二の脳」と呼ばれるのか? 内臓を動かす平滑筋の謎 —

棚橋 靖行 准教授
京都産業大学 生命科学部 先端生命科学科
私たちの意志とは無関係に働く消化管や膀胱。これらの内臓の壁を構成する「平滑筋」は、消化管の運動や尿の排出といった生命維持に不可欠な機能を担っています。この平滑筋の機能に異常が起きると、過敏性腸症候群や過活動膀胱といった病気に繋がります。
棚橋研究室は、「”くすり”を駆使して未知の生命現象を解き明かす」薬理学の手法を用いて、この精巧な調節メカニズムの解明に挑んでいます。
特に注目しているのが消化管です。消化管の運動は、自律神経だけでなく、「第二の脳」と呼ばれるほど複雑な「腸神経系」や、ペースメーカー細胞(カハール間質細胞:ICC)などによって精密に制御されています。さらに、「尿をためる(蓄尿)」と「尿を出す(排尿)」という相反する機能を持つ膀胱の研究も推進しています。

“くすり”や遺伝子改変マウスを用い、組織が「伸ばされた」ことを感知して開くイオンチャネル(イオンを通す門)など未解明の調節機構について、パッチクランプ法(細胞の電流を測定する手法)などの専門技術を用いて解析しています。
これらの正常な仕組みを徹底的に解明することが、原因不明の病気のメカニズムを明らかにし、新たな治療薬の開発に繋がります。
「RNAは“遺伝情報の中間体”に過ぎないのか?」
— 生命を操る「RNA制御」の原理を解き明かす —

三嶋 雄一郎 教授
京都産業大学 生命科学部 先端生命科学科
DNAが「生命の設計図」なら、タンパク質は「体を作る部品」です。その仲立ちをするメッセンジャーRNA(mRNA)は、単なる“中間体”なのでしょうか?
三嶋教授は「答えはNoだ」と言います。mRNAはむしろ、部品を作るための「発注書」です。生命は、この「発注書」を巧みに管理しています。適切なタイミングで発注(合成)し、不要になれば速やかに廃棄(分解)する。この精密な「RNA制御」こそが、生命活動の根幹を支えています。
もし、この制御メカニズムが狂えば、それが病気の原因にもなると考えられています。

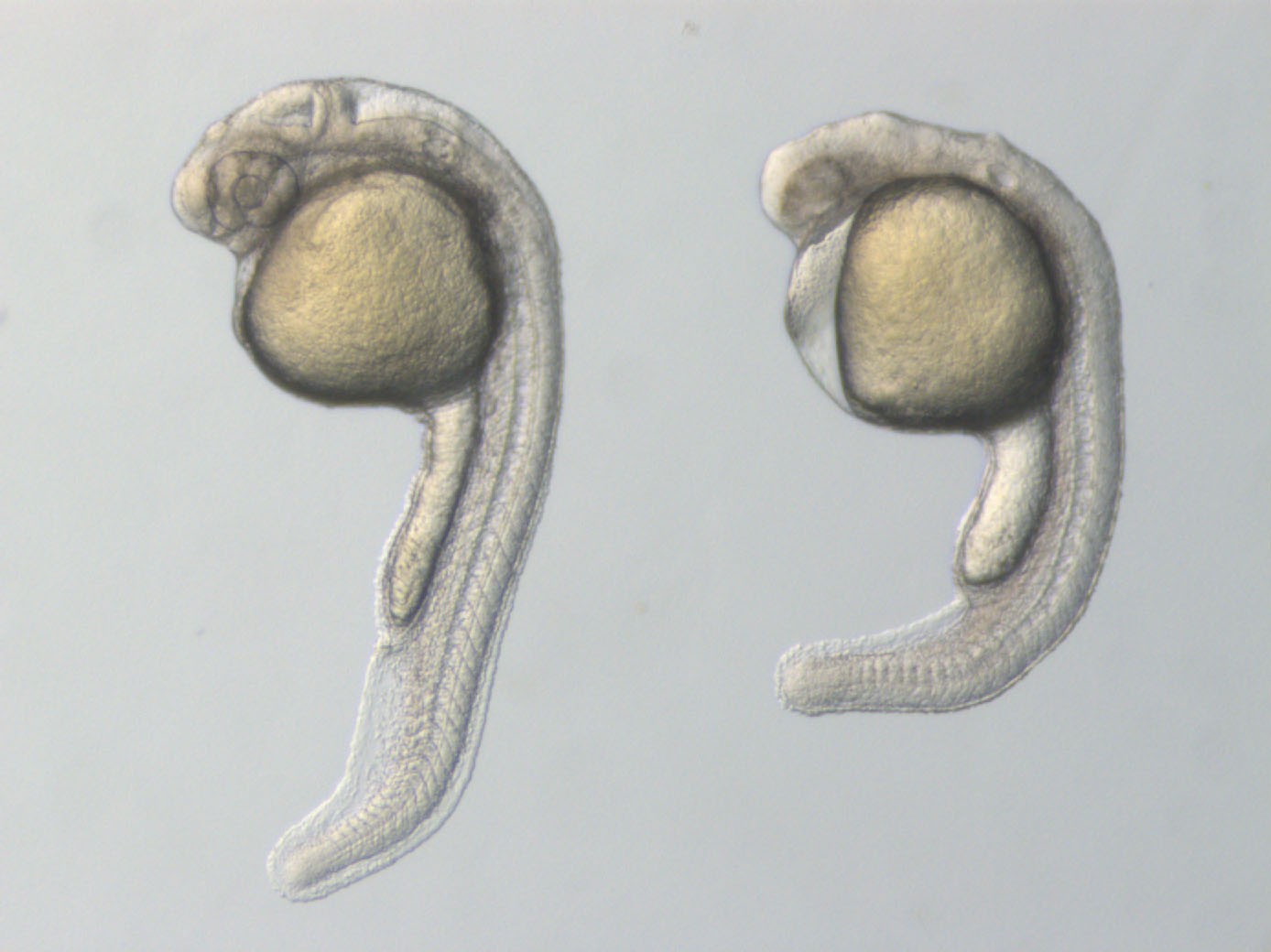
三嶋教授の研究室では、遺伝学の優れたモデルである「ゼブラフィッシュ」を用いて、この「RNA制御」の根本原理の解明に取り組んでいます。
ゲノム編集や次世代シークエンスといった最先端技術を駆使し、RNAの制御に異常が起きると個体の発生に何が起こるのかを解析。「未知のRNA制御機構」を発見しようとするこの基礎研究は、将来的にヒトの疾患の原因解明や、まったく新しい治療法の開発につながると期待されています。
「なぜ私たちの細胞には『死』のプログラムが備わっているのか?」
— 37兆個の「細胞社会」の秩序を守る、細胞死の謎に迫る —

川根 公樹 准教授
京都産業大学 生命科学部 先端生命科学科
私たちの体は37兆個の細胞からなる「細胞社会」です。毎日3000億個もの細胞が生まれ、同数の細胞が死ぬことで健康が保たれています。この「プログラムされた細胞死(アポトーシス)」は、胎児の手(水かき)が指になる時や、がん細胞の排除にも不可欠です。このバランスが崩れると、がんやアルツハイマー病などの疾患に繋がります。
これまでの研究は「死ぬ細胞」単体に着目していましたが、川根准教授は「細胞社会学」の視点から、死ぬ細胞が周囲とどう協力するかに注目しています。
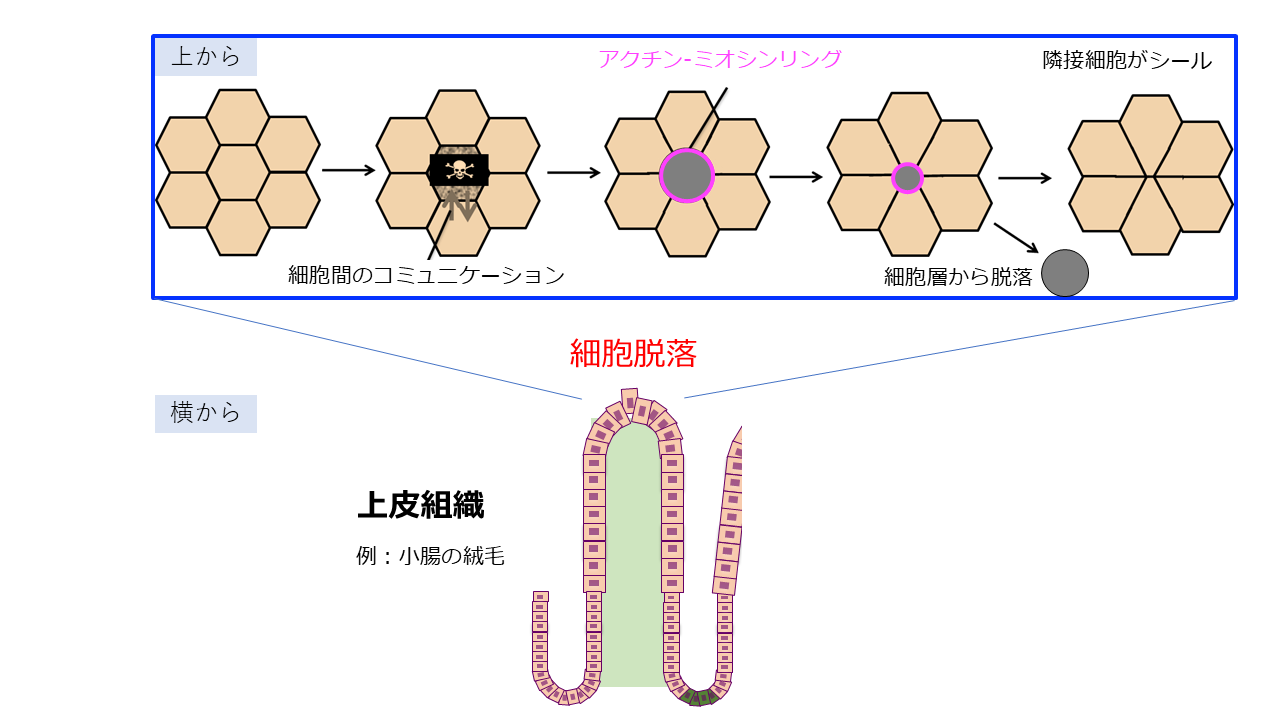
特に、細胞の入れ替わりが激しい腸の上皮(腸管)に着目。古い細胞が組織から脱落する「細胞脱落」の仕組みを研究しています。ライブセルイメージング(生きた細胞の動画撮影)を用いた研究で 、驚くべき協調メカニズムを発見。死ぬ細胞は自ら一部をちぎって小胞を作るだけでなく 、隣の細胞もリングを作って死ぬ細胞を「絞り出す」ように押し出すことを突き止めました。
この「細胞死の社会性」の解明は、がんや炎症性疾患の新たな治療法開発や、健康長寿の実現に貢献すると期待されます。
「ヒアルロン酸合成酵素の活性を高めて老化と戦う」
— 人類普遍のテーマ、健康長寿の実現へ向けて —

板野 直樹 教授
京都産業大学 生命科学部 先端生命科学科
高齢化社会の大きな問題「寝たきり」。その一因が、加齢による関節機能の低下(変形性関節症など)です。関節でクッションや潤滑剤としてはたらく「ヒアルロン酸」は年齢とともに急激に減少します。
ヒアルロン酸が減少すると、関節を動かしにくくなるだけでなく、炎症や痛みを伴い、やがて寝たきりの原因となります。症状の緩和・改善には、関節内に直接ヒアルロン酸を注射で補充する治療を受ける必要があります。しかし、体内で代謝されるため定期的な治療が必要です。
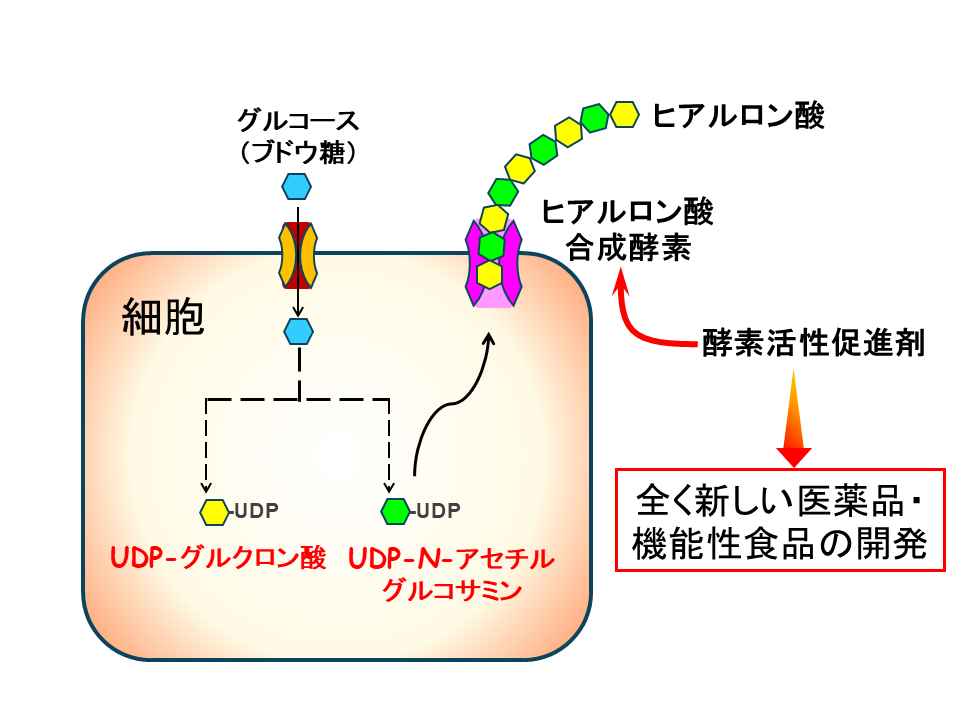
この課題に対し、板野教授は「動物体内でヒアルロン酸を作り出す酵素(ヒアルロン酸合成酵素)」の遺伝子クローニングに、世界で初めて成功しました。
この発見で合成メカニズムの解明は大きく前進。現在板野教授は、加齢で衰える合成能力を再び高める(=酵素を活性化させる)薬品や、機能性食品の探索を進めています。これ見つかれば、注射に頼る対症療法ではなく、病気を予防し、根本から治療する新しい医療や医薬品の開発に繋がります。
「寝たきり」という社会課題に挑む研究は、「健康寿命の延伸」に直結しています。
「なぜ“不良品”のタンパク質が病気を引き起こすのか」
— 細胞が持つ巧妙な「品質管理」の謎を解き、治療法開発へ —

潮田 亮 教授
京都産業大学 生命科学部 先端生命科学科
アルツハイマー病や糖尿病は、細胞内で作られるタンパク質の「不良品」が蓄積することが疾患の一因とされています。
私たちの体ではおよそ10万種のタンパク質が「誕生」「成熟」「死(分解)」という“一生”を循環しています。幸い、細胞には「タンパク質品質管理」という仕組みがあり、不良品を検知して分解することで病気を防いでいます。しかし、この仕組みが破綻すると様々な疾患を発症することになります。
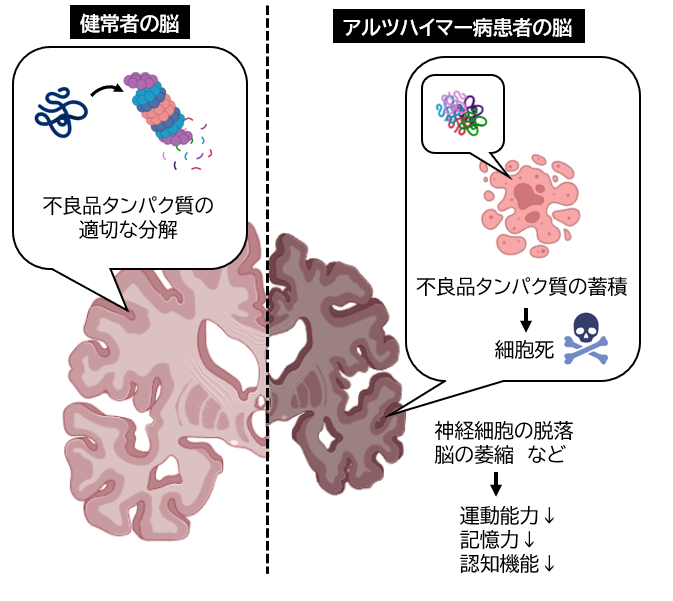
では、細胞はどのように不良品を見分け、分解しているのでしょうか。潮田教授は、まさにこの「分解のメカニズム」の解明に焦点を当てています。
ヒトの細胞やマウス、さらには「線虫」という小さな生物を使い、タンパク質の“一生”を実験室で観察し、品質管理の核心に迫っています。
この「不良品が分解される仕組み」を解き明かすことは、関連する病気の新たな治療法や創薬の開発に直結します。研究室では製薬・化粧品会社との共同研究も盛んで、基礎研究の成果をいち早く社会実装へとつなげる応用研究にも挑戦しています。







